Hoxe, o concepto coñecido como PRP apareceu por primeira vez no campo da hematoloxía na década de 1970.Os hematólogos crearon o termo PRP hai décadas para describir o plasma obtido a partir dun reconto de plaquetas superior ao valor básico do sangue periférico.Máis de dez anos despois, o PRP utilizouse na cirurxía maxilofacial como unha forma de fibrina rica en plaquetas (PRF).O contido de fibrina neste derivado de PRP ten un valor importante debido á súa adhesividade e ás súas características de estado estacionario, mentres que o PRP ten propiedades antiinflamatorias sostidas e estimula a proliferación celular.Finalmente, ao redor da década de 1990, o PRP comezou a facerse popular.Finalmente, esta tecnoloxía foi transferida a outros campos médicos.Desde entón, este tipo de bioloxía positiva foi amplamente estudada e aplicada ao tratamento de diversas lesións musculoesqueléticas de deportistas profesionais, o que promoveu aínda máis a súa atención xeneralizada nos medios de comunicación.Ademais de ser eficaz en ortopedia e medicina deportiva, o PRP tamén se utiliza en oftalmoloxía, xinecoloxía, uroloxía e cardioloxía, pediatría e cirurxía plástica.Nos últimos anos, o PRP tamén foi eloxiado polos dermatólogos polo seu potencial no tratamento de úlceras cutáneas, reparación de cicatrices, rexeneración de tecidos, rexuvenecemento da pel e incluso a perda de cabelo.
Tendo en conta o feito de que o PRP pode manipular directamente os procesos de cicatrización e inflamación, é necesario introducir a fervenza de curación como referencia.O proceso de curación divídese nas seguintes catro etapas: hemostase;Inflamación;Proliferación celular e matricial, e finalmente remodelación da ferida.
Curación de tecidos
Actívase a reacción en cascada de cicatrización dos tecidos, o que leva á agregación plaquetaria A formación de coágulos e o desenvolvemento da matriz extracelular temporal (ECM).Entón, as plaquetas adhírense ao coláxeno exposto e á proteína ECM, provocando a liberación de moléculas bioactivas presentes nos gránulos a.As plaquetas conteñen unha variedade de moléculas bioactivas, incluíndo factores de crecemento, factores de quimioterapia e citocinas, así como mediadores proinflamatorios, como prostaglandina, ciclina prostática, histamina, tromboxano, serotonina e bradicinina.
A fase final do proceso de cicatrización depende da remodelación da ferida.A remodelación do tecido está estrictamente regulada para establecer un equilibrio entre as reaccións anabólicas e catabólicas.Nesta fase, o factor de crecemento derivado das plaquetas (PDGF) e o factor de crecemento transformante (TGF-β) A fibronectina e a fibronectina estimulan a proliferación e migración de fibroblastos, así como a síntese de compoñentes de ECM.Non obstante, o tempo de maduración da ferida depende en gran medida da gravidade da ferida, das características individuais e da capacidade de curación específica do tecido ferido.Algúns factores fisiopatolóxicos e metabólicos poden afectar o proceso de curación, como a isquemia tisular, a hipoxia, a infección, o desequilibrio do factor de crecemento e incluso as enfermidades relacionadas coa síndrome metabólica.
O microambiente proinflamatorio interfire co proceso de curación.Máis complicado é que a alta actividade protease inhibe a acción natural do factor de crecemento (GF).Ademais das súas propiedades mitóticas, anxioxénicas e quimiotácticas, o PRP tamén é unha rica fonte de moitos factores de crecemento.Estas biomoléculas poden contrarrestar os efectos nocivos nos tecidos inflamatorios controlando o aumento da inflamación e establecendo estímulos anabólicos.Tendo en conta estas características, os investigadores poden atopar un gran potencial no tratamento de varias lesións complexas.
Moitas enfermidades, especialmente as de natureza musculoesquelética, dependen en gran medida de produtos biolóxicos que regulan o proceso inflamatorio, como o PRP para o tratamento da artrose.Neste caso, a saúde da cartilaxe articular depende do equilibrio preciso das reaccións anabolizantes e catabólicas.Tendo presente este principio, o uso de certos axentes biolóxicos positivos pode resultar exitoso para conseguir un equilibrio saudable.PRP porque libera plaquetas α- Os factores de crecemento contidos nos gránulos úsanse amplamente para regular o potencial de transformación do tecido, o que tamén reduce a dor.De feito, un dos principais obxectivos do tratamento con PRP é deter o principal microambiente inflamatorio e catabólico e promover a transformación en fármacos antiinflamatorios.Outros autores demostraron previamente que o PRP activado por trombina aumenta a liberación de varias moléculas biolóxicas.Estes factores inclúen o factor de crecemento do hepatocito (HGF) e o factor de necrose tumoral (TNF-α), o factor de crecemento transformante beta1 (TGF-β 1), o factor de crecemento endotelial vascular (VEGF) e o factor de crecemento da epiderme (EGF).Outros estudos demostraron que o PRP promove o aumento dos niveis de coláxeno tipo II e ARNm agrecano, mentres que reduce a inhibición da citocina proinflamatoria interleucina - (IL) 1 sobre eles.Tamén se suxeriu que debido a HGF e TNF-α [28] PRP pode axudar a establecer un efecto antiinflamatorio.Ambas estas preparacións moleculares reducen a actividade e expresión do factor nuclear kappaB (NF- κВ);En segundo lugar, a través da expresión de TGF-β 1 tamén impide a quimiotaxis dos monocitos, contrarrestando así o efecto do TNF-α sobre a transactivación das quimiocinas.O HGF parece desempeñar un papel indispensable no efecto antiinflamatorio inducido polo PRP.Esta potente citocina antiinflamatoria destrúe a vía de sinalización de NF-κ B e a expresión de citocinas proinflamatorias inhibe a resposta inflamatoria.Ademais, o PRP tamén pode reducir o alto nivel de óxido nítrico (NO).Por exemplo, na cartilaxe articular, demostrouse que o aumento da concentración de NO inhibe a síntese de coláxeno e induce a apoptose dos condrocitos, ao tempo que aumenta a síntese de metaloproteinases da matriz (MMPs), promovendo así a transformación do catabolismo.En termos de dexeneración celular, tamén se considera que o PRP é capaz de manipular a autofaxia de tipos celulares específicos.Ao alcanzar o estado final de envellecemento, algúns grupos celulares perden o potencial de estado estático e de auto renovación.Non obstante, estudos recentes demostraron que o tratamento con PRP pode reverter estas condicións daniñas.Moussa e os seus colegas demostraron que o PRP pode inducir a protección dos condrocitos aumentando os marcadores de autofaxia e antiinflamatorios, mentres que reduce a apoptose da cartilaxe da artrose humana.García Pratt et al.Infórmase de que a autofaxia determina a transición entre o destino de repouso e o envellecemento das células nai musculares.Os investigadores cren que, in vivo, a normalización da autofaxia integrada evita a acumulación de danos intracelulares e evita o envellecemento e o declive funcional das células satélites.Incluso nas células nai humanas envellecidas, como recentemente, Parrish e Rodes tamén fixeron contribucións significativas, revelando aínda máis o potencial antiinflamatorio do PRP.Nesta ocasión, o foco está na interacción entre plaquetas e neutrófilos.Na súa investigación, os investigadores explicaron que as plaquetas activadas liberadas polo ácido araquidónico foron absorbidas polos neutrófilos e convertéronse en leucotrienos e prostaglandinas, que son coñecidas moléculas inflamatorias.Non obstante, a interacción dos neutrófilos plaquetarios permite converter os leucotrienos en lipoproteínas, que se demostrou que son unha proteína antiinflamatoria eficaz que pode limitar a activación dos neutrófilos e previr a diálise e promover a herdanza ata a fase final da fervenza de curación.
O microambiente proinflamatorio interfire co proceso de curación.Máis complicado é que a alta actividade protease inhibe a acción natural do factor de crecemento (GF).Ademais das súas propiedades mitóticas, anxioxénicas e quimiotácticas, o PRP tamén é unha rica fonte de moitos factores de crecemento.Estas biomoléculas poden contrarrestar os efectos nocivos nos tecidos inflamatorios controlando o aumento da inflamación e establecendo estimulación anabólica.
Factor celular
As citocinas no PRP xogan un papel fundamental na manipulación do proceso de reparación dos tecidos e na regulación do dano inflamatorio.As citocinas antiinflamatorias son unha ampla gama de moléculas bioquímicas que median na resposta das citocinas proinflamatorias, inducidas principalmente por macrófagos activados.As citocinas antiinflamatorias interactúan con inhibidores específicos de citocinas e receptores de citocinas solubles para regular a inflamación.Interleucina (IL) - 1 antagonistas do receptor, IL-4, IL-10, IL-11 e IL-13 clasifícanse como os principais fármacos antiinflamatorios, as citocinas.Segundo os diferentes tipos de feridas, algunhas citocinas, como interferón, factor inhibidor da leucemia, TGF-β e IL-6, que poden mostrar efectos proinflamatorios ou antiinflamatorios.O TNF-α、 IL-1 e IL-18 teñen certos receptores de citocinas, que poden inhibir o efecto proinflamatorio doutras proteínas [37].A IL-10 é unha das citocinas antiinflamatorias máis eficaces, que pode regular á baixa as citocinas proinflamatorias como a IL-1, a IL-6 e o TNF-α, e a aumentar os factores antiinflamatorios.Estes mecanismos antireguladores xogan un papel fundamental na produción e función de citocinas proinflamatorias.Ademais, certas citocinas poden desencadear respostas de sinal específicos para estimular os fibroblastos, que son fundamentais para a reparación dos tecidos.A citocina inflamatoria TGF β 1 、 IL-1 β 、 IL-6, IL-13 e IL-33 estimulan os fibroblastos a diferenciarse en miofibroblastos e mellorar a ECM [38].Pola súa banda, os fibroblastos segregan citocinas TGF- β 、 IL-1 β 、 IL-33, CXC e CC quimiocinas promoven a resposta inflamatoria activando e recrutando células inmunes como os macrófagos.Estas células inflamatorias desempeñan múltiples funcións na ferida, principalmente promovendo a eliminación da ferida e a biosíntese de quimiocinas, metabolitos e factores de crecemento, que é crucial para a reconstrución de novos tecidos.Polo tanto, as citocinas no PRP xogan un papel importante na estimulación da resposta inmune mediada por tipos celulares e na promoción da regresión da fase inflamatoria.De feito, algúns investigadores designaron este proceso como "inflamación rexenerativa", indicando que a fase inflamatoria, a pesar da ansiedade do paciente, é un paso necesario e crítico para a conclusión exitosa do proceso de reparación do tecido, tendo en conta o mecanismo epixenético que sinala a inflamación. promover a plasticidade celular.
O papel das citocinas na inflamación da pel fetal é de gran importancia para a investigación da medicina rexenerativa.A diferenza entre os mecanismos de curación fetal e adulto é que os tecidos fetais danados ás veces volven ao seu estado orixinal segundo a idade do feto e os tipos de tecidos relevantes.Nos humanos, a pel do feto pode rexenerarse completamente en 24 semanas, mentres que nos adultos, a cicatrización das feridas pode provocar a formación de cicatrices.Como sabemos, en comparación cos tecidos sans, as propiedades mecánicas dos tecidos cicatriciais redúcense significativamente e as súas funcións son limitadas.Préstase especial atención á citocina IL-10, que se atopa moi expresada no líquido amniótico e na pel do feto, e demostrouse que desempeña un papel na reparación sen cicatrices da pel do feto, promovida polo efecto pleiotrópico da citocina.ZgheibC et al.Estudouse o transplante de pel fetal en ratos IL-10 transxénicos knockout (KO) e ratos control.Os ratos IL-10KO mostraron signos de inflamación e formación de cicatrices ao redor dos enxertos, mentres que os enxertos do grupo control non mostraron cambios significativos nas propiedades biomecánicas nin cicatrizarse.
A importancia de regular o delicado equilibrio entre a expresión de citocinas antiinflamatorias e proinflamatorias é que estas últimas, cando se producen en exceso, envían finalmente sinais de degradación celular ao reducir a expresión de certos xenes.Por exemplo, na medicina musculoesquelética, IL-1 β Down regula SOX9, que é responsable do desenvolvemento da cartilaxe.SOX9 produce importantes factores de transcrición para o desenvolvemento da cartilaxe, regula o coláxeno tipo II alfa 1 (Col2A1) e é responsable de codificar os xenes de coláxeno tipo II.IL-1 β Finalmente, diminuíu a expresión de Col2A1 e agrecano.Non obstante, demostrouse que o tratamento con produtos ricos en plaquetas inhibe a IL-1 β. Aínda é un aliado factible da medicina rexenerativa para manter a expresión dos xenes codificadores de coláxeno e reducir a apoptose dos condrocitos inducida por citocinas proinflamatorias.
Estimulación anabólica: ademais de regular o estado inflamatorio do tecido danado, as citocinas do PRP tamén participan na reacción anabólica xogando os seus papeis de mitose, atracción química e proliferación.Este é un estudo in vitro liderado por Cavallo et al.Estudar os efectos de diferentes PRP nos condrocitos humanos.Os investigadores observaron que os produtos PRP con concentracións de plaquetas e leucocitos relativamente baixas estimulan a actividade normal dos condrocitos, o que favorece a promoción dalgúns mecanismos celulares de resposta anabólica.Por exemplo, observouse a expresión do coláxeno tipo ii e dos glicanos agregados.Pola contra, as altas concentracións de plaquetas e leucocitos parecen estimular outras vías de sinalización celular que implican varias citocinas.Os autores suxiren que isto pode deberse á presenza dunha gran cantidade de glóbulos brancos nesta formulación particular de PRP.Estas células parecen ser responsables do aumento da expresión de certos factores de crecemento, como VEGF, FGF-b e interleucinas IL-1b e IL-6, que á súa vez poden estimular TIMP-1 e IL-10.Noutras palabras, en comparación coa fórmula de PRP "mala", a mestura de PRP rica en plaquetas e glóbulos brancos parece promover a relativa invasividade dos condrocitos.
Un estudo deseñado por Schnabel et al.foi deseñado para avaliar o papel dos biomateriais autólogos no tecido do tendón do cabalo.Os autores recolleron mostras de sangue e tendóns de seis cabalos adultos novos (2-4 anos) e centráronse no estudo do patrón de expresión xénica, o contido de ADN e coláxeno dos explantes de tendóns do flexor digitorum superficialis de cabalos cultivados no medio que contén PRP. ou outros produtos sanguíneos.Cultiváronse os explantes de tendóns en sangue, plasma, PRP, plasma deficiente plaquetario (PPP) ou aspirados de medula ósea (BMA) e engadíronse aminoácidos a DMEM libre de soro 100%, 50% ou 10%.Ao realizar a análise bioquímica aplicable despois de..., os investigadores observaron que TGF-β A concentración de PDGF-BB e PDGF-1 no medio PRP era especialmente maior que a de todos os outros produtos sanguíneos probados.Ademais, os tecidos de tendón cultivados en medio 100% PRP mostraron un aumento da expresión xénica das proteínas da matriz COL1A1, COL3A1 e COMP, pero non aumentaron os encimas catabólicos MMPs3 e 13. Polo menos en termos de estrutura do tendón, este estudo in vivo apoia o uso de autolo - un produto sanguíneo gotoso, ou PRP, para o tratamento da tendinite de grandes mamíferos.
Chen et al.O efecto reconstrutivo do PRP foi máis discutido.Na súa serie anterior de estudos, os investigadores demostraron que, ademais de mellorar a formación de cartilaxe, o PRP tamén promoveu o aumento da síntese de ECM e inhibiu a reacción inflamatoria da cartilaxe articular e do núcleo pulposo.O PRP pode activar o TGF mediante a fosforilación de Smad2/3-. A vía do sinal β xoga un papel importante no crecemento e diferenciación celular.Ademais, tamén se cre que os coágulos de fibrina formados despois da activación do PRP proporcionan unha estrutura tridimensional sólida, que permite que as células se adhiran, o que pode levar á construción de novos tecidos.
Outros investigadores fixeron contribucións significativas ao tratamento das úlceras cutáneas crónicas no campo da dermatoloxía.Isto tamén é salientable.Por exemplo, a investigación realizada por Hessler e Shyam en 2019 mostra que o PRP é valioso como un tratamento alternativo factible e eficaz, mentres que a úlcera crónica resistente aos medicamentos aínda supón unha carga económica importante para a atención sanitaria.En particular, a úlcera dos pés da diabetes é un problema de saúde importante ben coñecido, o que fai que as extremidades sexan fáciles de amputar.Un estudo publicado por Ahmed et al.en 2017 demostrou que o xel de PRP autólogo podería estimular a cicatrización de feridas en pacientes con úlcera crónica do pé por diabetes liberando os factores de crecemento necesarios, mellorando así significativamente a taxa de cicatrización.Do mesmo xeito, Gonchar e os seus colegas revisaron e discutiron o potencial rexenerativo dos cócteles de PRP e factores de crecemento para mellorar o tratamento das úlceras dos pés da diabetes.Os investigadores propuxeron que o uso de mesturas de factores de crecemento é probable que sexa unha posible solución, que pode mellorar as vantaxes do uso de PRP e factor de crecemento único.Polo tanto, en comparación co uso dun único factor de crecemento, a combinación de PRP e outras estratexias de tratamento pode promover significativamente a curación das úlceras crónicas.
Fibrina
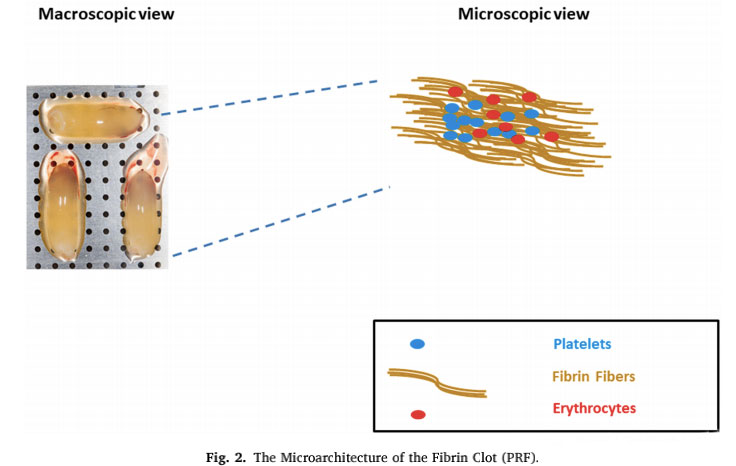
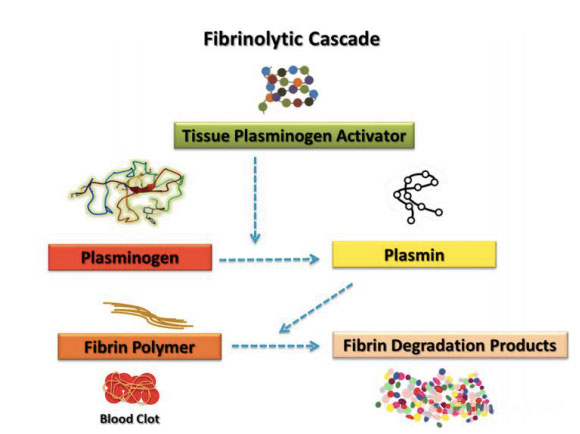
As plaquetas levan varios factores relacionados co sistema fibrinolítico, que poden regular a alza ou a baixar a reacción fibrinolítica.A relación temporal e a contribución relativa dos compoñentes hematolóxicos e da función plaquetaria na degradación do coágulo segue sendo un problema digno de unha ampla discusión na comunidade.A literatura introduce moitos estudos que só se centran nas plaquetas, que son famosas pola súa capacidade para afectar o proceso de curación.A pesar dun gran número de estudos destacados, outros compoñentes hematolóxicos, como os factores de coagulación e os sistemas fibrinolíticos, tamén se descubriron que contribúen significativamente á reparación eficaz da ferida.Por definición, a fibrinólise é un proceso biolóxico complexo que depende da activación de certos encimas para favorecer a degradación da fibrina.A reacción de fibrinólise foi proposta por outros autores que os produtos de degradación da fibrina (fdp) poden ser realmente axentes moleculares responsables de estimular a reparación do tecido.A secuencia de eventos biolóxicos importantes antes é da deposición de fibrina e a eliminación da anxioxénese, que é necesaria para a cicatrización das feridas.A formación de coágulos despois da lesión serve como capa protectora para protexer os tecidos da perda de sangue e da invasión de axentes microbianos, e tamén proporciona unha matriz temporal a través da cal as células poden migrar durante o proceso de reparación.O coágulo débese a que o fibrinóxeno é escindido pola serina protease e as plaquetas reúnense na malla de fibras de fibrina entrecruzada.Esta reacción provocou a polimerización do monómero de fibrina, que é o principal evento de formación de coágulos sanguíneos.O coágulo tamén se pode usar como reservorio de citocinas e factores de crecemento, que se liberan durante a desgranulación das plaquetas activadas.O sistema fibrinolítico está estrictamente regulado pola plasmina, e xoga un papel fundamental na promoción da migración celular, a biodisponibilidade dos factores de crecemento e a regulación doutros sistemas de protease implicados na inflamación e rexeneración dos tecidos.Os compoñentes clave da fibrinólise, como o receptor do activador do plasminóxeno da uroquinase (uPAR) e o inhibidor do activador do plasminóxeno-1 (PAI-1), sábese que se expresan en células nai mesenquimales (MSC), que son tipos de células especiais necesarios para a cicatrización exitosa de feridas. .
Migración celular
A activación do plasminóxeno mediante a asociación uPA uPAR é un proceso que promove a migración das células inflamatorias porque mellora a proteólise extracelular.Debido á falta de dominios transmembrana e intracelular, uPAR necesita co receptores como integrina e vitelina para regular a migración celular.Ademais, indicou que a unión de uPA uPAR deu lugar a un aumento da afinidade de uPAR pola vitrectonectina e a integrina, o que promoveu a adhesión celular.O inhibidor do activador do plasminóxeno-1 (PAI-1) á súa vez fai que as células se desprendan.Cando se une ao uPA do complexo de integrina upar uPA na superficie celular, destrúe a interacción entre a vitelina upar e a vitelina integrina.
No contexto da medicina rexenerativa, as células nai mesenquimatosas da medula ósea mobilízanse a partir da medula ósea no caso de danos orgánicos graves, polo que poden atoparse na circulación de pacientes con fracturas múltiples.Non obstante, en casos específicos, como a insuficiencia renal terminal, a insuficiencia hepática terminal ou durante o rexeitamento despois do transplante cardíaco, é posible que estas células non se detecten no sangue [66].Curiosamente, estas células proxenitoras mesenquimales (estromales) derivadas da medula ósea humana non se puideron detectar no sangue de individuos sans [67].O papel da uPAR na mobilización de células nai mesenquimatosas da medula ósea (BMSC) propúxose previamente, o que é similar á aparición de uPAR na mobilización de células nai hematopoéticas (HSC).Varabaneni et al.Os resultados mostraron que o uso de factor estimulante de colonias de granulocitos en ratos con deficiencia de uPAR provocou o fallo do MSC, o que volveu reforzar o papel de apoio do sistema de fibrinólise na migración celular.Outros estudos tamén mostraron que os receptores uPA ancorados con glicosil fosfatidilinositol regulan a adhesión, a migración, a proliferación e a diferenciación activando certas vías de sinalización intracelulares, como segue: vías de sinalización de fosfatidilinositol 4,5-difosfato 3-quinase/Akt e ERK1/2 supervivebles e quinase de adhesión. (FAK).
No contexto da cicatrización de feridas MSC, o factor fibrinolítico demostrou a súa importancia.Por exemplo, os ratos con deficiencia de plasminóxeno mostraron un grave atraso nos eventos de cicatrización de feridas, o que indica que a plasmina era importante neste proceso.Nos humanos, a perda de plasmina tamén pode provocar complicacións na cicatrización das feridas.A interrupción do fluxo sanguíneo pode inhibir significativamente a rexeneración dos tecidos, o que tamén explica por que estes procesos de rexeneración son máis difíciles en pacientes con diabetes.
As células nai mesenquimatosas de medula ósea foron recrutadas no lugar da ferida para acelerar a cicatrización da ferida.En condicións estables, estas células expresaban uPAuPAR e PAI-1.As dúas últimas proteínas son factores inducibles por hipoxia α (HIF-1 α) A orientación é moi conveniente porque HIF-1 nas MSC α A activación de FGF-2 e HGF promoveu a regulación á alza de FGF-2 e HGF;HIF-2 α Á súa vez, o VEGF-A [77] está regulado positivamente, o que contribúe á cicatrización das feridas.Ademais, o HGF parece mellorar o recrutamento de células nai mesenquimatosas da medula ósea nos sitios da ferida dunha forma sinérxica.Hai que ter en conta que as condicións isquémicas e hipóxicas interfiren significativamente coa reparación da ferida.Aínda que as BMSC tenden a vivir en tecidos que proporcionan baixos niveis de osíxeno, a supervivencia das BMSC transplantadas in vivo tórnase limitada porque as células transplantadas adoitan morren en condicións adversas observadas nos tecidos danados.O destino da adhesión e supervivencia das células nai mesenquimatosas da medula ósea baixo hipoxia depende dos factores fibrinolíticos secretados por estas células.O PAI-1 ten unha alta afinidade pola vitelina, polo que pode competir pola unión de uPAR e integrina á vitelina, inhibindo así a adhesión e migración celular.
Sistema de monocitos e rexeneración
Segundo a literatura, hai moitas discusións sobre o papel dos monocitos na cicatrización de feridas.Os macrófagos proceden principalmente de monocitos sanguíneos e xogan un papel importante na medicina rexenerativa [81].Debido a que os neutrófilos segregan IL-4, IL-1, IL-6 e TNF-α, estas células adoitan penetrar na ferida unhas 24-48 horas despois da lesión.As plaquetas liberan trombina e factor plaquetario 4 (PF4), que poden promover o recrutamento de monocitos e diferenciarse en macrófagos e células dendríticas.Unha característica importante dos macrófagos é a súa plasticidade, é dicir, poden converter fenotipos e diferenciarse noutros tipos celulares, como as células endoteliais, e despois mostrar diferentes funcións a diferentes estímulos bioquímicos no microambiente da ferida.As células inflamatorias expresan dous fenotipos principais, M1 ou M2, dependendo do sinal molecular local como fonte de estimulación.Os macrófagos M1 son inducidos por axentes microbianos, polo que teñen máis efectos proinflamatorios.Pola contra, os macrófagos M2 adoitan producirse por reaccións de tipo 2 e teñen propiedades antiinflamatorias, normalmente caracterizadas por un aumento de IL-4, IL-5, IL-9 e IL-13.Tamén participa na reparación dos tecidos mediante a produción de factores de crecemento.A transición do subtipo M1 ao M2 está en gran parte impulsada pola fase tardía da cicatrización das feridas.Os macrófagos M1 desencadean a apoptose dos neutrófilos e inician a eliminación destas células).A fagocitose dos neutrófilos activa unha serie de eventos, nos que se desactiva a produción de citocinas, polarizando macrófagos e liberando TGF-β 1。 Este factor de crecemento é un regulador clave da diferenciación dos miofibroblastos e da contracción da ferida, o que permite a resolución da inflamación e o inicio da fase de proliferación na fervenza de curación [57].Outra proteína moi relacionada implicada nos procesos celulares é a serina (SG).Este proteoglicano de gránulos secretores de células hematopoyéticas descubriuse que é necesario para almacenar proteínas secretoras en células inmunitarias específicas, como mastocitos, neutrófilos e linfocitos T citotóxicos.Aínda que moitas células non hematopoéticas tamén sintetizan plasminóxeno, todas as células inflamatorias producen unha gran cantidade desta proteína e almacénana en gránulos para unha maior interacción con outros mediadores inflamatorios, incluíndo proteases, citocinas, quimiocinas e factores de crecemento.As cadeas de glicosaminoglicanos cargadas negativamente (GAG) en SG parecen ser críticas para a estabilidade dos gránulos secretores, xa que poden unirse e facilitar o almacenamento de compoñentes granulares esencialmente cargados nunha célula, proteína e cadea GAG de forma específica.Respecto da súa participación na investigación sobre PRP, Woulfe e os seus colegas demostraron previamente que a deficiencia de SG está estreitamente relacionada cos cambios morfolóxicos das plaquetas;Factor plaquetario 4 β- Defectos do almacenamento de PDGF na tromboglobulina e as plaquetas;Mala agregación e secreción plaquetaria in vitro e trombose in vivo.Polo tanto, os investigadores concluíron que este proteoglicano parece ser o principal regulador da trombose.
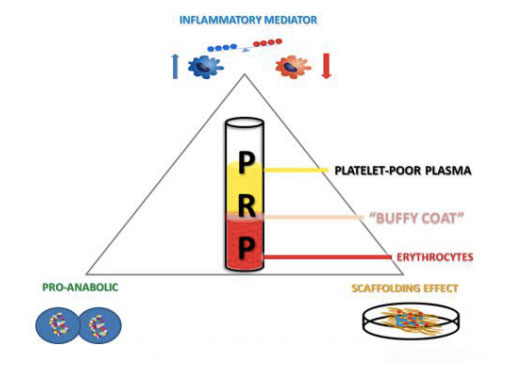
Os produtos ricos en plaquetas poden obter sangue total persoal mediante a recollida e centrifugación, e dividir a mestura en diferentes capas que conteñen plasma, plaquetas, glóbulos brancos e glóbulos brancos.Cando a concentración de plaquetas é superior ao valor básico, pode acelerar o crecemento do óso e dos tecidos brandos, con menos efectos secundarios.A aplicación de produtos PRP autólogos é unha biotecnoloxía relativamente nova, que mostrou continuamente resultados optimistas para estimular e mellorar a cicatrización de varias lesións dos tecidos.A eficacia deste método de tratamento alternativo pódese atribuír á entrega local dunha ampla gama de factores de crecemento e proteínas para simular e apoiar o proceso de cicatrización fisiolóxica de feridas e reparación de tecidos.Ademais, o sistema fibrinolítico obviamente ten unha influencia importante na reparación do tecido completo.Ademais de cambiar o recrutamento celular das células inflamatorias e das células nai mesenquimatosas da medula ósea, tamén pode regular a actividade proteolítica das áreas de cicatrización de feridas e o proceso de rexeneración dos tecidos mesodérmicos, incluíndo ósos, cartilaxe e músculos, polo que é un compoñente clave de medicina musculoesquelética.
A curación acelerada é o obxectivo moi perseguido por moitos profesionais do ámbito médico.O PRP representa unha ferramenta biolóxica positiva, que segue proporcionando un desenvolvemento prometedor para estimular e coordinar a fervenza de eventos rexenerativos.Non obstante, debido a que esta ferramenta terapéutica aínda é moi complexa, especialmente porque libera innumerables factores bioactivos e os seus diversos mecanismos de interacción e efectos de transdución de sinais, é necesario investigar máis.
(Os contidos deste artigo son reimpresos e non ofrecemos ningunha garantía expresa ou implícita sobre a exactitude, fiabilidade ou integridade dos contidos deste artigo, e non somos responsables das opinións deste artigo, por favor entendelo.)
Hora de publicación: 16-12-2022